研究摘要|Summary
國防醫學院與陽明交通大學研究團隊最新發表於 Journal of Dental Sciences(2025)的研究證實, PDL® 雷射微通道鈦表面可活化牙齦間質幹細胞(GMSC), 促進 CCN1 與 EDIL3 的分泌,進而加速血管新生與早期骨整合。 本研究以 16 位人類來源細胞、細胞外囊泡分析及 3D 血管生成類器官模型完整驗證其生物機制, 為 PDL® 植體提供具高度臨床意義的科學實證。
國防醫學院與國立陽明交通大學、臺大牙醫部等研究團隊最新發表於 Journal of Dental Sciences(2025)的研究顯示, 雷射微米通道(laser-modified microchannels)鈦表面 能顯著提升牙齦間質幹細胞(GMSC)的血管生成能力, 並透過細胞外囊泡(EVs)釋放關鍵因子 CCN1 與 EDIL3,加速植體周圍微血管形成,進一步提升早期骨整合與軟組織穩定性。
研究背景:血管新生是影響早期穩定度的關鍵
植牙成功率不僅仰賴骨整合,也高度依賴植體周圍的微循環與軟組織品質。充足的微血管供應與良好的免疫調節能力,有助於:
- 提供氧氣與營養,支持早期骨修復與重塑
- 協助清除發炎介質與代謝廢物
- 建立穩定的軟組織封合,降低細菌侵入風險
近年研究指出,植體表面微結構 可直接影響細胞貼附、排列與基因表現。本研究即比較三種鈦表面: 機械加工(machined)、SLA(sand-blasted, large-grit, acid-etched)與雷射微通道(laser-modified microchannels), 探討其對人體 GMSC 及血管新生的影響。
雷射微通道提供最佳細胞附著與排列
研究使用商用純鈦(grade IV)製作圓盤,並分別處理為機械面、SLA 及雷射微通道表面。雷射處理以 DPSS Nd:YVO4 雷射 在鈦表面形成寬度約 約 10–17 μm 的微通道,為細胞提供方向性的拓撲結構。

掃描電子顯微鏡結果顯示,GMSC 在雷射微通道表面呈現梭狀延展並沿溝槽排列,相較於機械面與 SLA 上較為圓潤分散的形態, 代表雷射微通道能提供更佳的貼附深度與細胞張力,為後續血管新生與骨整合奠定良好基礎。
雷射微通道啟動 CCN1 與 EDIL3 基因表現與染色質開放度
研究團隊使用 ATAC-seq 與 RNA-seq 分析 GMSC 在不同鈦表面上的染色質可及性與基因表現,發現雷射微通道可顯著提升多個與血管新生、 細胞遷移相關的基因,其中以 CCN1(CYR61)與 EDIL3 最為關鍵。
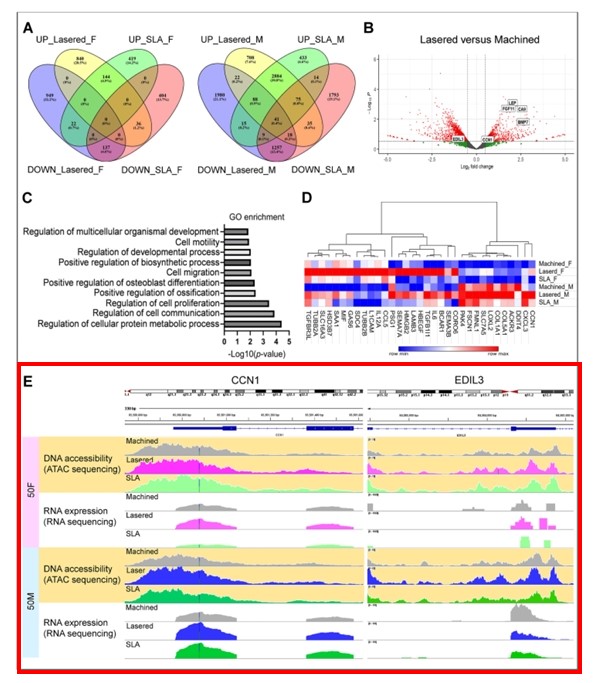
這些結果顯示,雷射微通道並非僅是「粗糙化表面」,而是能主動啟動 GMSC 內部訊息傳遞的 生物活性拓撲訊號(bioactive topographical cues),驅動血管新生相關基因網路。
細胞外囊泡中的 CCN1 / EDIL3 與性別差異(Sex-dimorphic Response)
為進一步釐清 GMSC 如何將這些訊號傳遞至血管內皮細胞,研究團隊將培養上清分離為細胞外囊泡(EV)與非 EV 分畫, 並以 ELISA 與 Western blot 檢測 CCN1 與 EDIL3 含量。
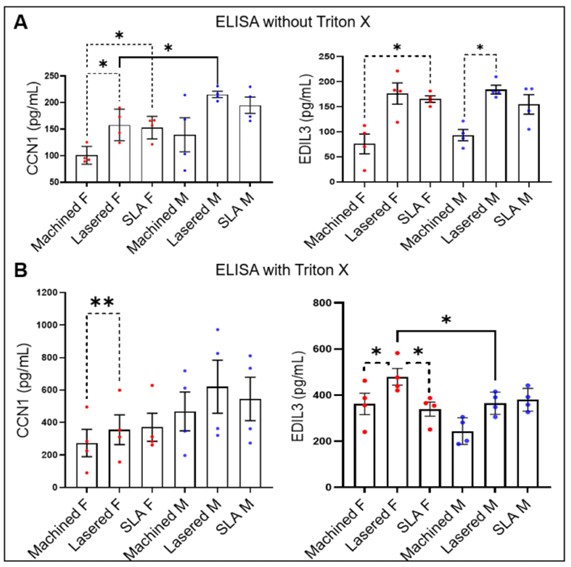
研究結果顯示:
- 男性 GMSC 在雷射微通道上分泌較多 CCN1,與骨整合與血管新生密切相關。
- 女性 GMSC 則分泌較多 EDIL3,與免疫調節與炎症消退(inflammation resolution)有關。
這是首次證實人體 GMSC 對植體表面存在性別差異(sex-dimorphic)的生物反應,顯示植體表面設計可能與病患本身的生物學性別產生交互作用。
條件培養基證實:雷射微通道最能促進血管新生
研究利用 GMSC 在三種鈦表面培養 72 小時後所獲得的條件培養基(GMSC-conditioned medium), 刺激人類臍靜脈內皮細胞(HUVEC),並於基質膠上進行 72 小時的 tube formation 測試。
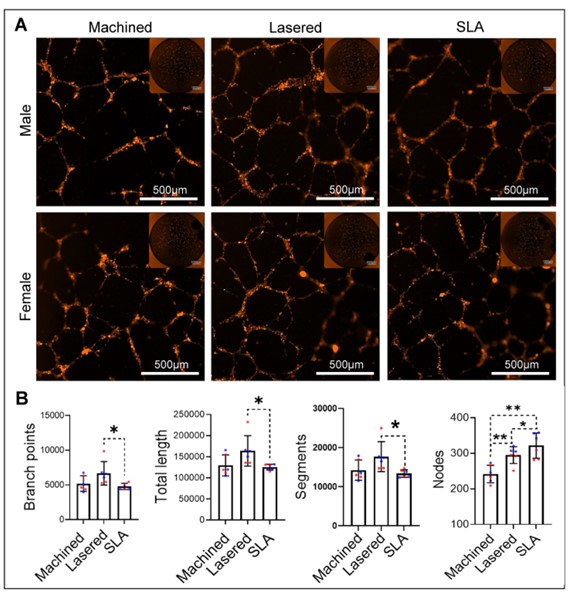
結果顯示,相較於機械面與 SLA,雷射微通道組別的 HUVEC 形成了更多且更長的微血管網路, 在分支點(branch points)、總長度(total length)、segments 及 nodes 等指標上均顯著提升。
3D 類器官模型:雷射微通道周圍形成最完整的微血管網
為更貼近臨床植體周圍微環境,研究團隊建立 3D 血管生成類器官模型:將 GMSC 與 GelMA 混合, 再嵌入具有機械面、雷射微通道或 SLA 表面的鈦棒,之後於表面加入 HUVEC,觀察其三維血管生成狀態。
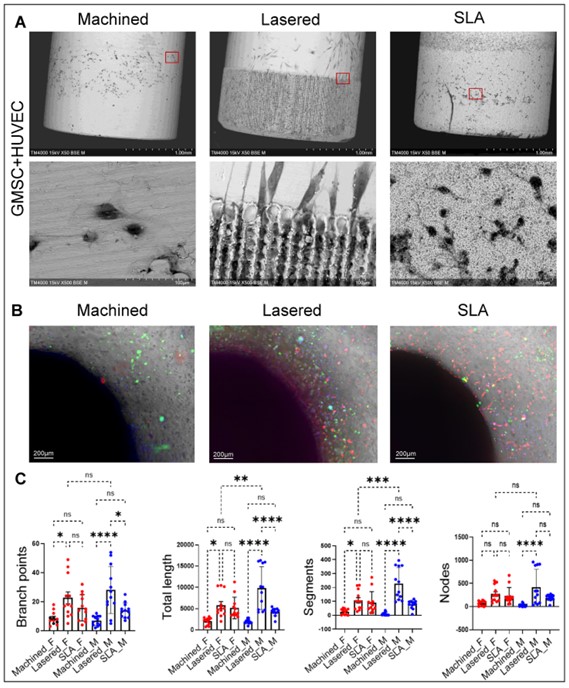
在此模型中,雷射微通道組別不論在血管長度、分支數、節點數皆優於機械面與 SLA,進一步驗證其對早期血管生成的促進效果。
臨床意義:更好的血管生成=更可預期的早期骨整合
血管生成是植體早期穩定與長期成功的關鍵前提。PDL® 雷射微通道鈦表面能:
- 啟動 GMSC 分泌促血管生成因子 CCN1 與 EDIL3,並透過 EV 傳遞至內皮細胞
- 加速植體周圍微血管網路建立,改善局部微循環
- 支持軟組織封合與早期骨整合,降低初期失敗風險
對臨床醫師而言,這代表:更快速的初期穩定、更佳的骨整合可預期性,以及更長期穩定的植牙成果。
原始研究連結與引用資訊
研究標題:Laser-modified titanium surfaces induce sex-dimorphic secretion of angiogenic factors by gingiva-derived mesenchymal stromal cells
發表期刊:Journal of Dental Sciences(2025)
DOI:https://doi.org/10.1016/j.jds.2025.09.013

